
新闻中心
【原创】CMV 特异性T细胞检测在造血干细胞移植中的应用
巨细胞病毒(Cytomegalovirus,简称CMV),为人疱疹病毒5型,能够在人体建立终身持续感染,可导致人群广泛感染,其感染率高达70%-100%。在造血干细胞和器官移植领域,由于人群较高的CMV感染率,患者自身可能携带CMV,移植组织或者器官也可能携带CMV。造血干细胞移植(haematopoietic stem cell transplant,HSCT)后,为了预防免疫排斥反应的发生,提高移植成功率,临床上会使用免疫抑制剂来抑制免疫系统的功能,此时受者体内或者外源移植物中潜伏感染的CMV病毒重新激活。移植患者的CMV感染/激活发生率可达80%,可发展为CMV疾病,造成患者的不同器官损伤,具有高的病死率。尽管预防或抢先治疗已经得到广泛应用,仍有2-17%的患者发生CMV疾病[1-2]。目前,CMV病毒感染相关检测包括CMV核酸和CMV抗体检测等方法。
实时定量PCR(RT-qPCR)检测CMV-DNA:CMV病毒载量可以采用定量PCR法测定病毒DNA拷贝数,目前是CMV病毒血症和CMV病的一种常见临床诊断手段。其中血标本RT-qPCR因其高敏感性,成为CMV病毒血症首选的诊断技术。但RT-qPCR也存在一些局限性,如检测方法尚未统一,不同检测技术的结果具有较大差异。
CMV特异IgG 和 IgM抗体检测:通过ELISA等方法检测CMV特异IgM抗体和IgG抗体水平可提示感染状态。但是,CMV特异抗体水平免疫检测反映的是体液免疫,而CMV病毒的清除则需要细胞免疫中病毒特异效应T细胞发挥靶细胞杀伤作用。另一方面,CMV特异抗体水平免疫检测虽然可用于辅助诊断CMV病毒感染状态,但是存在抗体滴度随时间变化和细胞的抗体分泌能力差异,因此抗体检测往往用于定性。
由于机体CMV特异的细胞免疫水平对CMV激活的长期控制至关重要,因此开发新的CMV特异免疫检测手段及时预测CMV感染风险并进行患者风险分层,提高移植手术成功率和延长患者生存期,对临床防治CMV感染具有较大的意义。
02、CMV特异性T细胞及其检测方法
CMV感染后,机体的固有免疫和适应性免疫应答先后被激活。在适应性免疫应答中,B细胞经过生发中心反应,高亲和力和特异性的细胞被选择,并大量克隆扩增,分泌抗体对抗病毒感染。同时,抗原提呈细胞或其他CMV感染的靶细胞表面的MHC分子结合并提呈加工处理后的CMV抗原短肽,会被CMV特异性CD4+辅助T细胞或CD8+ 细胞毒性T细胞的TCR特异识别,通过释放干扰素-γ (IFN-γ) 和肿瘤坏死因子-α (TNF-α)等细胞因子,或者直接杀伤靶细胞,来有效控制机体CMV病毒的活动感染。
T细胞免疫对于机体控制CMV复制和防止进展成为CMV疾病至关重要[3-7]。机体对CMV的清除主要依赖细胞免疫,尤其是CD8+细胞毒性T淋巴细胞(cytotoxic lymphocyte,CTL)对感染细胞的杀伤来完成,故CTL在抗CMV感染中起重要作用。如何更加精确的评估移植后患者对CMV特异性T细胞免疫状态,对指导抗CMV治疗有现实意义,有助于避免对所有移植后患者常规持续给予抗CMV药物而影响CMV特异性T细胞。CMV病毒载量检测联合CMV特异性T细胞免疫监测有利于了解机体防御CMV感染/激活的免疫保护能力,识别CMV临床相关并发症增加的患者。
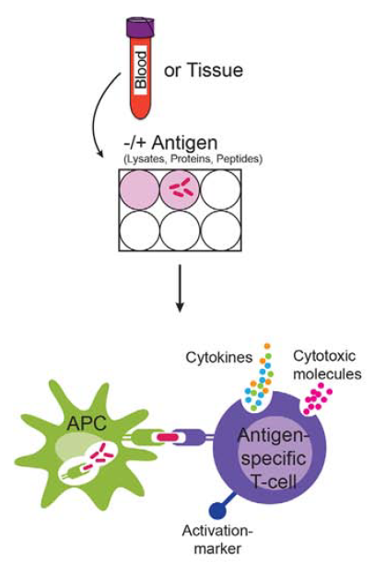
图 1 ELISpot实验原理
基于酶联免疫斑点实验(Enzyme-Linked ImmunoSpot Assay, ELISpot)的CMV ELISpot方法是一种快速的、高灵敏度的和单细胞水平的CMV抗原特异性T细胞免疫检测方法。由于在疫苗研发和免疫治疗等前沿领域,ELISpot检测的科学意义已被广泛认可并得以应用,因此成为CMV特异T细胞频数检测的可靠工具。具体原理是通过抗原递呈细胞表面的MHC分子递呈CMV抗原肽,与CMV特异性T细胞表面的TCR结合并相互作用产生细胞因子IFN-γ,用抗体捕获培养细胞分泌的细胞因子,并以酶联斑点显色的方式将其表现出来,通过酶联免疫斑点分析仪对斑点进行自动计数和分析,最终通过检测产生IFN-γ的细胞数目来评估CMV特异性T细胞免疫状态(图1)。
03、CMV特异性T细胞检测及临床意义
CMV ELISpot方法当前在移植领域广泛开展,在预测CMV感染发生风险,指导预防性抗病毒治疗方面显示了巨大的应用前景。
1.术后,监测CMV特异性T细胞免疫重建,提示发生CMV激活风险
在一项前瞻性多中心研究中,选取241例CMV血清状态阳性的同种异体造血干细胞移植受者,从移植前到移植后6个月通过CMV ELISpot检测评估CMV-CMI(CMV cell-mediated immunity)。结果显示,移植后低CMV特异性T细胞免疫反应(IE-1抗原刺激下分泌IFN-γ的T细胞频数≤50 SFCs/2.5×105 PBMCs)与CMV激活发生高风险有关(HR=3.37,95% CI = 1.04-10.93)(图2)。即在有CS-CMVi(clinically significant CMV infection)的患者中,CMV-CMI水平较低(94%)。
另几项研究中,对接受莱特莫韦预防的患者组和接受抢先治疗的患者组,分析了两组的移植物抗宿主病(GVHD)、中性粒细胞减少症、基线疾病复发率和总生存率。发现莱特莫韦预防会延迟CMV感染和CMV特异性免疫重建,需要在停止预防后实施免疫学和病毒学监测[4-6]。因此,应用T-SPOT.CMV检测CMV-CMI有助于临床监测allo-HCT受者的CMV特异细胞免疫水平变化,并区分需要抗病毒预防或治疗的CS-CMVi风险人群和受到保护的人群。
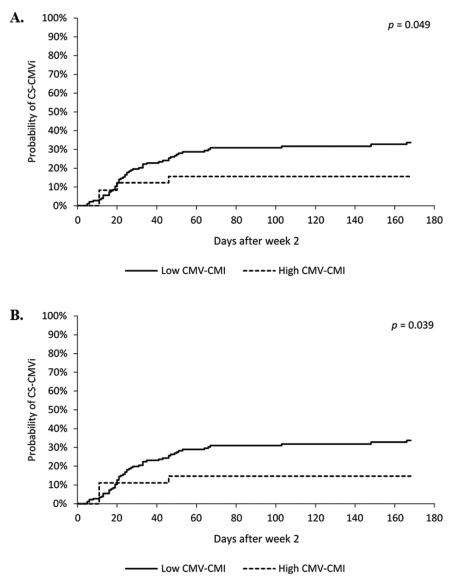
图 2 不同临界值下,CMV-CMI水平与CS-CMVi累积发生率
2.术后,联合CMV DNA载量检测结果,更好的帮助临床决定抗病毒治疗方案
在一项多中心HSCT患者抢先抗CMV处理的研究中,通过联合病毒学和免疫学的手段进行免疫监测,发现CMV免疫水平在接受抗病毒处理后30天内恢复至一定水平(定义为pp65/IE1特异性CD8+ T细胞水平>1 cell/ul)(图3),可以终止抗病毒治疗[6],在一定程度上减少了非必要的抗病毒治疗,潜在的避免了对移植患者的药物毒性,以及降低治疗费用。
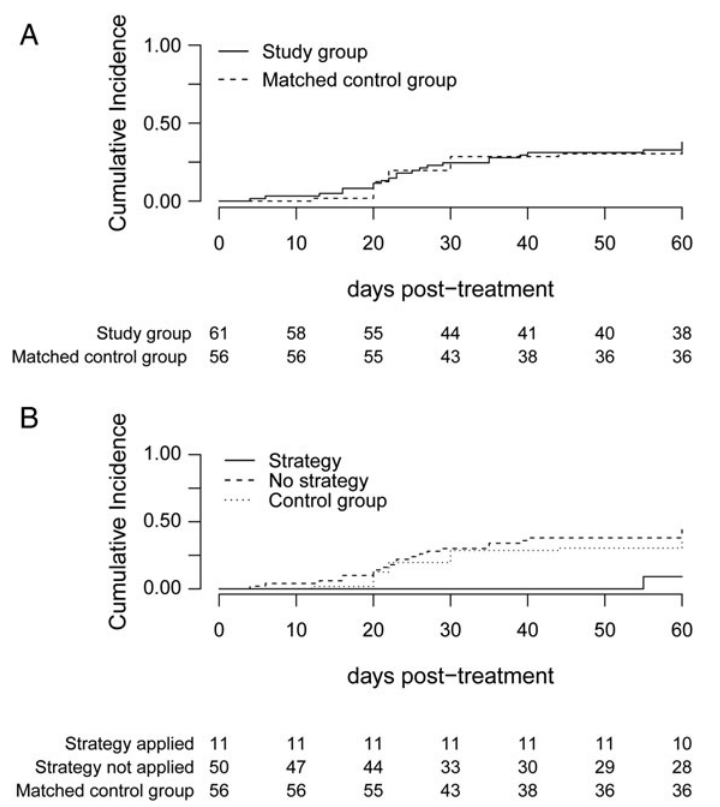
图 3 免疫学和病毒学监测指导抗病毒治疗后两个月内CMV DNAemia累积发生率
因此,CMV ELISpot免疫检测具备的高灵敏度、单细胞水平和绝对定量等优势,不仅在科研和医药研发领域发挥重要作用,也对造血干细胞移植后患者的病毒特异细胞免疫评价,移植和生存质量提升具有重要意义。CMV ELISpot免疫检测的推广,使得临床医师可以从免疫的角度评估病毒感染,助力“精准医学”目标的实现。
总结
CMV激活是异基因造血干细胞移植(allo-HSCT)受者发病和死亡的主要原因之一。细胞介导的免疫反应对于防止潜伏感染个体的CMV激活非常重要,并被认为是预防CMV复制的主要防御机制。
监测CMV特异性T细胞免疫可以反应异基因造血干细胞移植术后免疫重建情况,结合病毒载量检测,提示CMV复制和发展为CMV疾病的风险,更好的帮助临床决定抗病毒治疗方案。有利于减少CMV监测的持续时间和强度,减少在CMV感染风险较低的患者中抗CMV治疗的成本和药物副作用。
对于HSCT患者术后CMV激活的监测管理,荻硕贝肯可提供CMV DNA载量检测和CMV ELISpot检测,对术后CMV感染的防治策略具有重要的指导意义,也能使临床更加科学地管理CMV感染。
参考文献
[1]2023CSCO造血干细胞移植治疗血液系统疾病指南
[2]异基因造血干细胞移植患者巨细胞病毒感染管理中国专家共识(2022年版)
[3]Chemaly RF, El Haddad L, Winston DJ, et al. Cytomegalovirus (CMV) Cell-Mediated Immunity and CMV Infection After Allogeneic Hematopoietic Cell Transplantation: The REACT Study. Clin Infect Dis. 2020;71(9):2365-2374. doi:10.1093/cid/ciz1210
[4]Gabanti E, Borsani O, Colombo AA, et al. Human Cytomegalovirus-Specific T-Cell Reconstitution and Late-Onset Cytomegalovirus Infection in Hematopoietic Stem Cell Transplantation Recipients following Letermovir Prophylaxis. Transplant Cell Ther. 2022;28(4):211.e1-211.e9. doi:10.1016/j.jtct.2022.01.008
[5]Zavaglio F, Vitello D, Bergami F, et al. Human Cytomegalovirus (HCMV) – specific T-cell response after letermovir prophylaxis is predictive for subsequent HCMV reactivation in haematopoietic stem cell transplant recipients.
J Clin Virol. 2023;165:105519. doi:10.1016/j.jcv.2023.105519
[6]Navarro D, Amat P, de la Cámara R, et al. Efficacy and Safety of a Preemptive Antiviral Therapy Strategy Based on Combined Virological and Immunological Monitoring for Active Cytomegalovirus Infection in Allogeneic Stem Cell Transplant Recipients. Open Forum Infect Dis. 2016;3(2):ofw107. doi:10.1093/ofid/ofw107
[7]Yong MK, Lewin SR, Manuel O. Immune Monitoring for CMV in
Transplantation. Curr Infect Dis Rep. 2018;20(4):4. Published 2018 Mar 14. doi:10.1007/s11908-018-0610-4
(本网站所有标识“原创”的内容,均为荻硕贝肯原创,版权均归荻硕贝肯所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:荻硕贝肯官网”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)

